07 多模态数据分析
多模态单细胞技术在一个细胞里同时测两种信息:CITE-seq 同时测 RNA 和细胞表面蛋白,10x Multiome 同时测 RNA 和染色质可及性。相比纯 scRNA-seq,多模态数据的优势是可以相互验证和补充:RNA 层的聚类结果,往往能在蛋白层找到更清晰的 marker。
本节用 10x Genomics 的 5k PBMC CITE-seq 数据演示最常用的一条 CITE-seq 分析流程:分别标准化 RNA 和 ADT,再用 WNN(Weighted Nearest Neighbor)做联合聚类。
多模态技术对比
| 技术 | 测量内容 | 常见用途 |
|---|---|---|
| CITE-seq | RNA + 表面蛋白(ADT) | 免疫学、细胞分型 |
| ASAP-seq | RNA + 染色质开放 | 调控机制 |
| 10x Multiome | RNA + ATAC(同细胞) | 基因表达与调控联动 |
| Perturb-seq | RNA + CRISPR 扰动 | 遗传学筛选 |
CITE-seq 门槛低,直接用标准 Seurat/Scanpy 就能做;Multiome 需要走 Cell Ranger ARC 流程,后续分析借助 Signac 或 MultiVI。
CITE-seq 的 WNN 分析
数据是 01 章里�介绍过的 5k PBMC CITE-seq,下载后 filtered_feature_bc_matrix/ 目录里同时包含 Gene Expression 和 Antibody Capture 两层矩阵。
先读入并分别对两层数据做标准化和降维:
library(Seurat)
# 读取 CITE-seq 数据(同时包含 RNA 和 ADT)
data_dir <- "~/biof3-data/pbmc5k-citeseq/filtered_feature_bc_matrix"
counts <- Read10X(data.dir = data_dir)
# 创建 Seurat 对象:RNA 作为主 assay,ADT 作为额外 assay
cbmc <- CreateSeuratObject(counts = counts$`Gene Expression`, project = "PBMC5K_CITE")
cbmc[["ADT"]] <- CreateAssayObject(counts = counts$`Antibody Capture`)
# RNA 标准化 + 高变基因 + PCA
DefaultAssay(cbmc) <- "RNA"
cbmc <- NormalizeData(cbmc)
cbmc <- FindVariableFeatures(cbmc)
cbmc <- ScaleData(cbmc)
cbmc <- RunPCA(cbmc)
# ADT 用 CLR 归一化(Centered Log Ratio),更适合抗体信号
DefaultAssay(cbmc) <- "ADT"
cbmc <- NormalizeData(cbmc, normalization.method = "CLR", margin = 2)
cbmc <- ScaleData(cbmc)
cbmc <- RunPCA(cbmc, reduction.name = "apca")
RNA 和 ADT 的归一化方式不同:RNA 常用 LogNormalize,ADT 用 CLR(margin = 2 意为按细胞做 CLR)。两层分别做完 PCA 后,用 WNN 把它们的邻居结构加权合并,再在合并图上聚类和降维:
# WNN:根据两个 reduction 同时找邻居
cbmc <- FindMultiModalNeighbors(
cbmc,
reduction.list = list("pca", "apca"),
dims.list = list(1:30, 1:18)
)
# 在 WNN 图上做 UMAP 和聚类
cbmc <- RunUMAP(cbmc, nn.name = "weighted.nn", reduction.name = "wnn.umap")
cbmc <- FindClusters(cbmc, graph.name = "wsnn", resolution = 0.5)
# 可视化
DimPlot(cbmc, reduction = "wnn.umap", label = TRUE)
跑完得到的 cbmc@meta.data 里会新增一列 seurat_clusters,Reductions(cbmc) 里会多出 wnn.umap。比较三张 UMAP(只用 RNA、只用 ADT、WNN 联合)通常会看到:WNN 版本在分群边界上更干净,尤其是 T 细胞内部的 CD4/CD8 亚群。
真实示例:5k PBMC CITE-seq 走 WNN
配套脚本 module08_cite_seq_sci.R 把上面的流程完整跑了一遍,用的是 10x 官方 5k PBMC CITE-seq 数据(Gene Expression + 32 个抗体的 TotalSeq-B panel,~37 MB):
Rscript scripts/single-cell/sc08_citeseq_sci.R
脚本顺序跟上一节完全对上:Read10X 自动拆出两层矩阵 → 分别建 RNA 和 ADT assay → RNA 做 LogNormalize + PCA、ADT 做 CLR + PCA → FindMultiModalNeighbors 合并两个 reduction → 在 WNN 图上做 Leiden 聚类和 wnn.umap,同时单独留一份 rna.umap 和 adt.umap 用来对比。QC 之后大概留下 4000 多个细胞。
每张图看什么
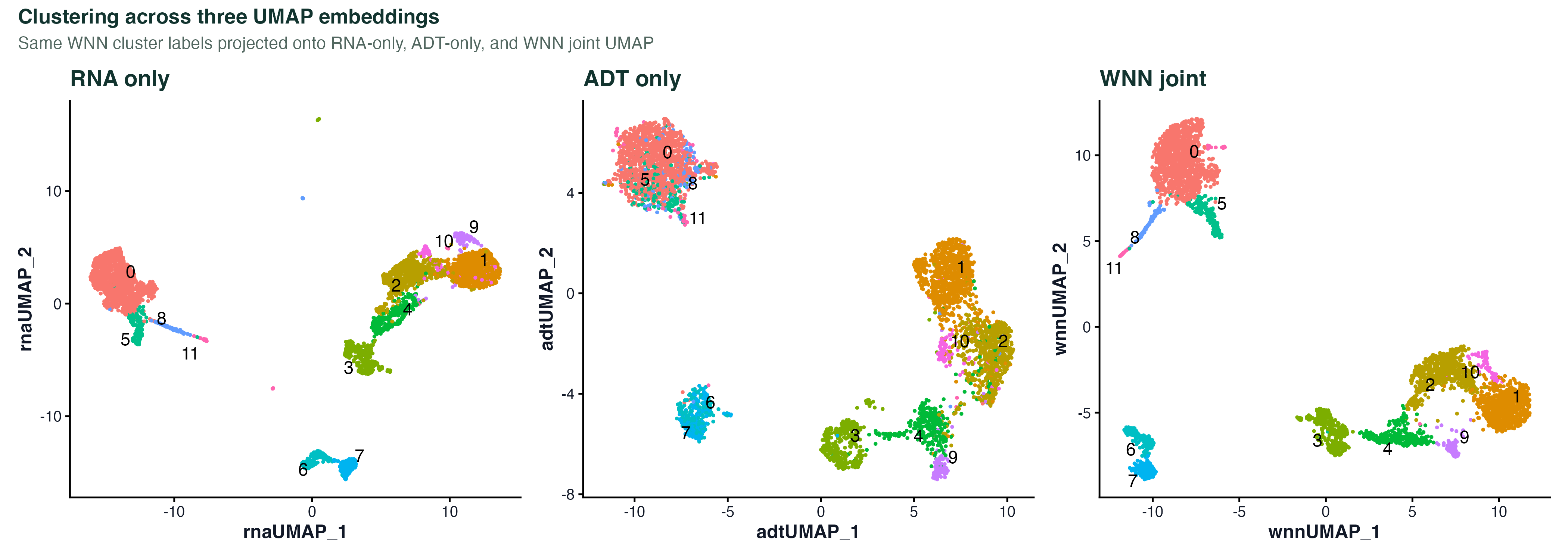
图 1:把同一份 WNN 聚类标签分别画到 RNA UMAP、ADT UMAP ��和 WNN UMAP 上。RNA UMAP 在小群细胞(DC、浆细胞样)上分得更细,ADT UMAP 对 T/B/单核大类的边界更干净,WNN 结合两边的优势,最终的 cluster 边界最整齐。
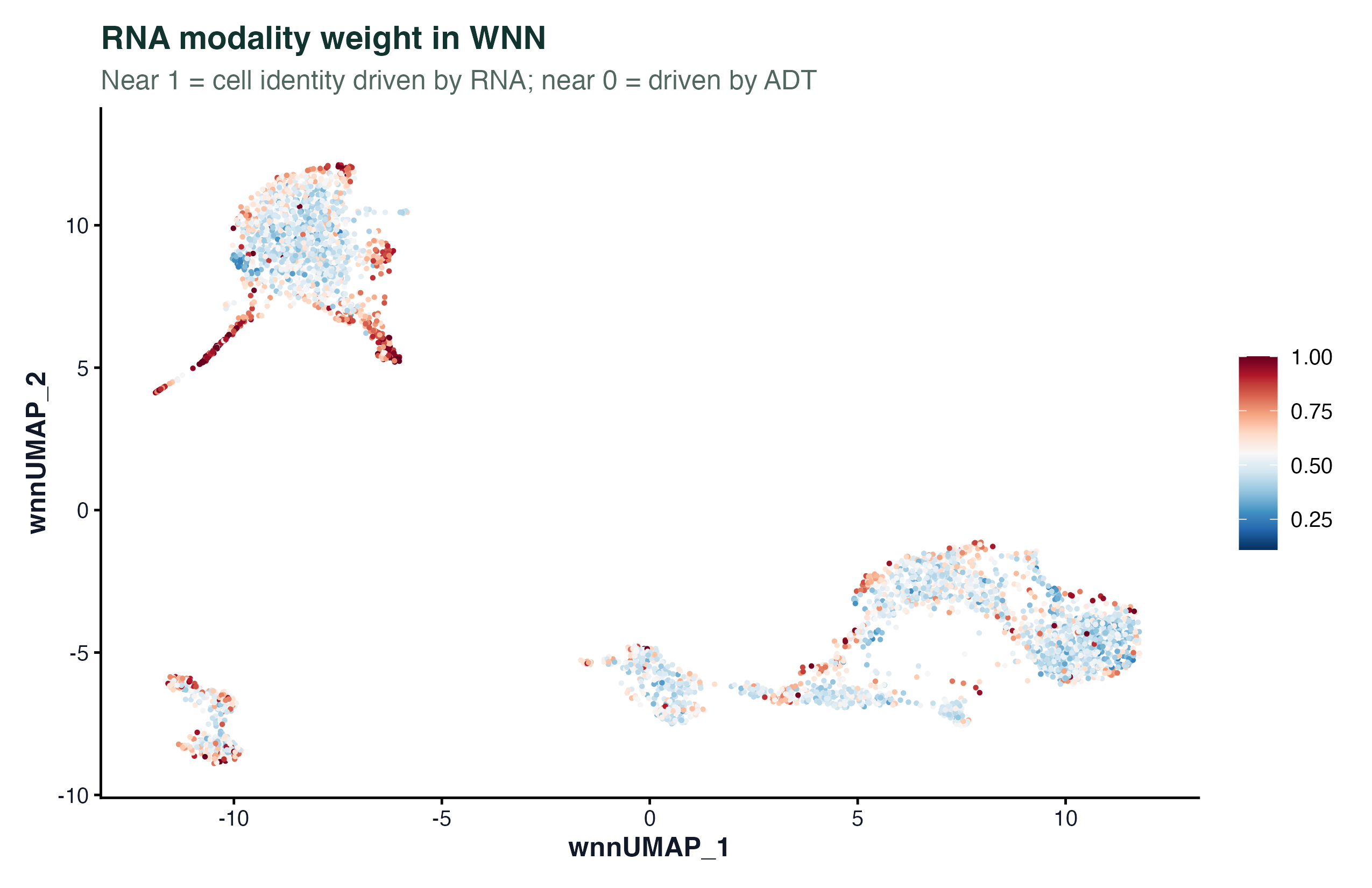
图 2:每个细胞在 WNN 邻居图里 RNA 的权重。接近 1 的区域主要靠 RNA 区分(像稀有亚群、发育状态相关的细胞),接近 0 的区域主要靠 ADT 区分(像成熟 T 细胞、单核细胞)。这张图是"WNN 不是简单平均"的最直观证据。
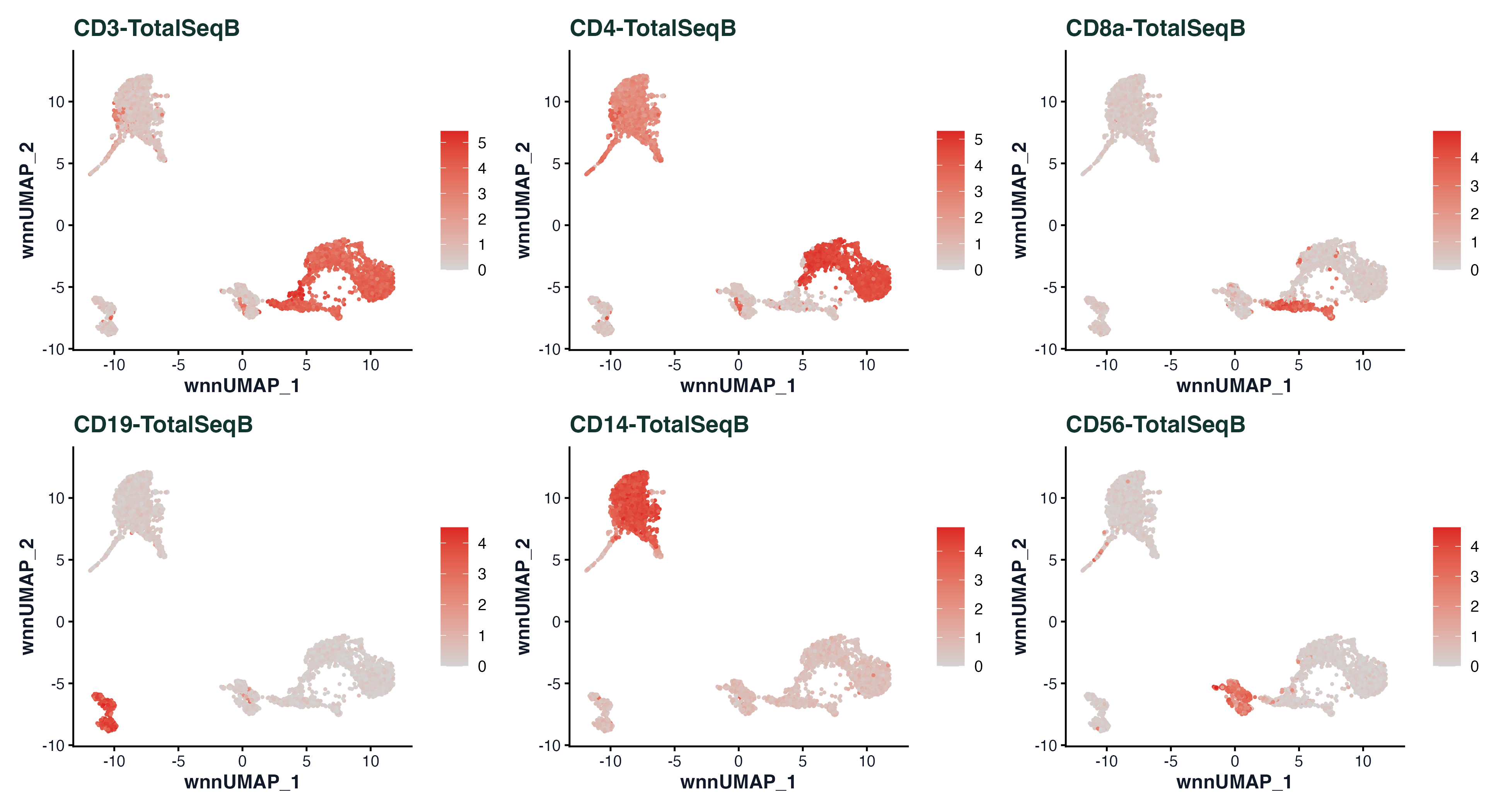
图 3:CD3、CD4、CD8、CD14、CD19、CD56 六个经典 marker 的 ADT 信号在 WNN UMAP 上的分布。CD3⁺ 的大块就是 T 细胞,其内部 CD4 和 CD8 分得很干净;CD19⁺ 对应 B 细胞;CD14⁺ 对应单核;CD56⁺ 对应 NK。不需要再额外做 marker 查询,这六张子图就能把 PBMC 的主要群体读出来。
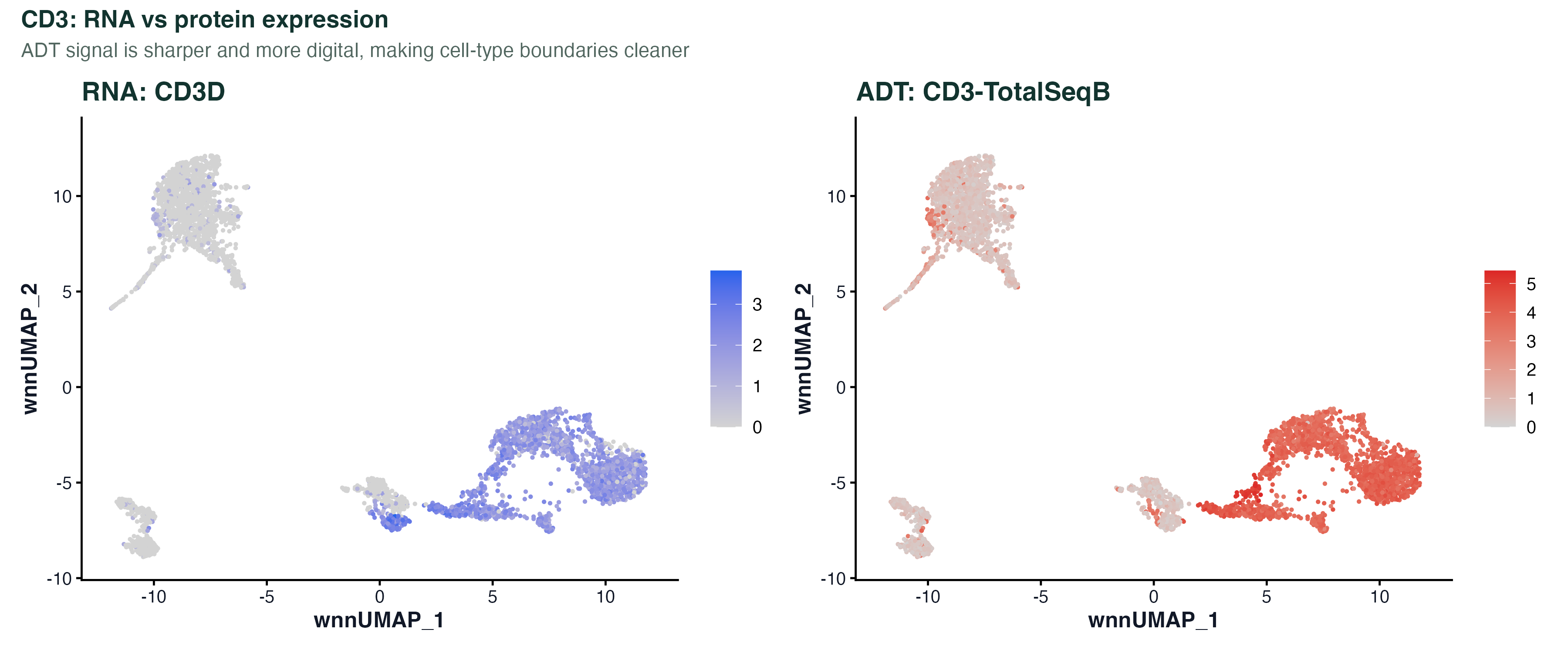
图 4:同一 WNN UMAP 上 CD3D(RNA 层)和 CD3-TotalSeqB(ADT 层)的表达对比。RNA 信号稀疏、有不少落在 T 细胞区的细胞读数为 0;ADT 信号连续、集中,边界非常锐利。这是 CITE-seq 最直接的价值:抗体信号稳定得多,做 T/非 T 的切分不会因为 dropout 误伤。
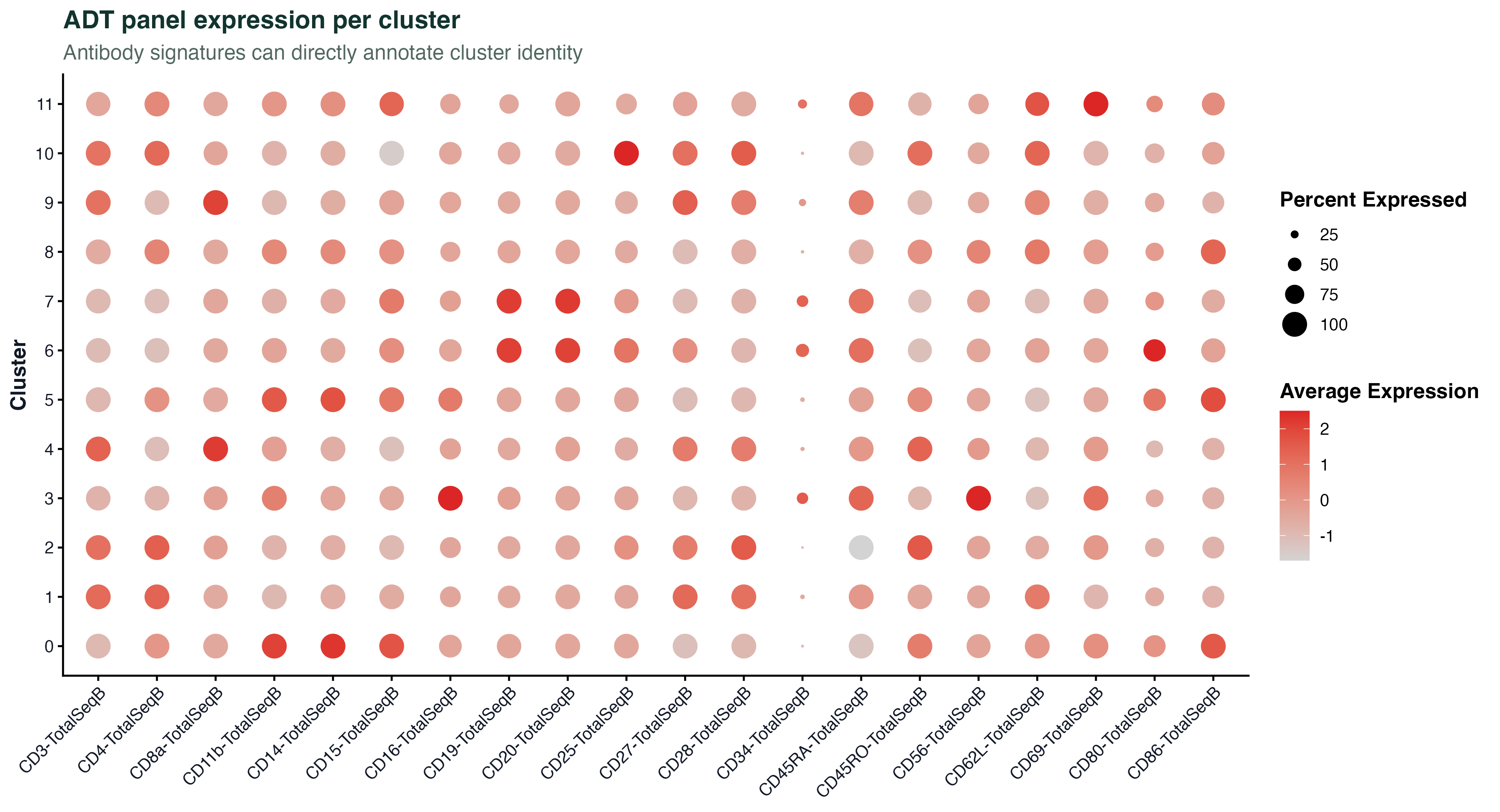
图 5:ADT panel 前 20 个抗体在每个 cluster 里的平均表达(颜色)和阳性细胞比例(点大小)。每个 cluster 对应的阳性抗体组合一看就懂:CD3/CD4/CD45RA 是 naive CD4 T,CD3/CD8/CD45RO 是 memory CD8 T,CD14/CD11b 是经典单核,CD19/CD20 是 B,依此类推。真实项目里直接看这张图就能把大部分 cluster 命名掉。
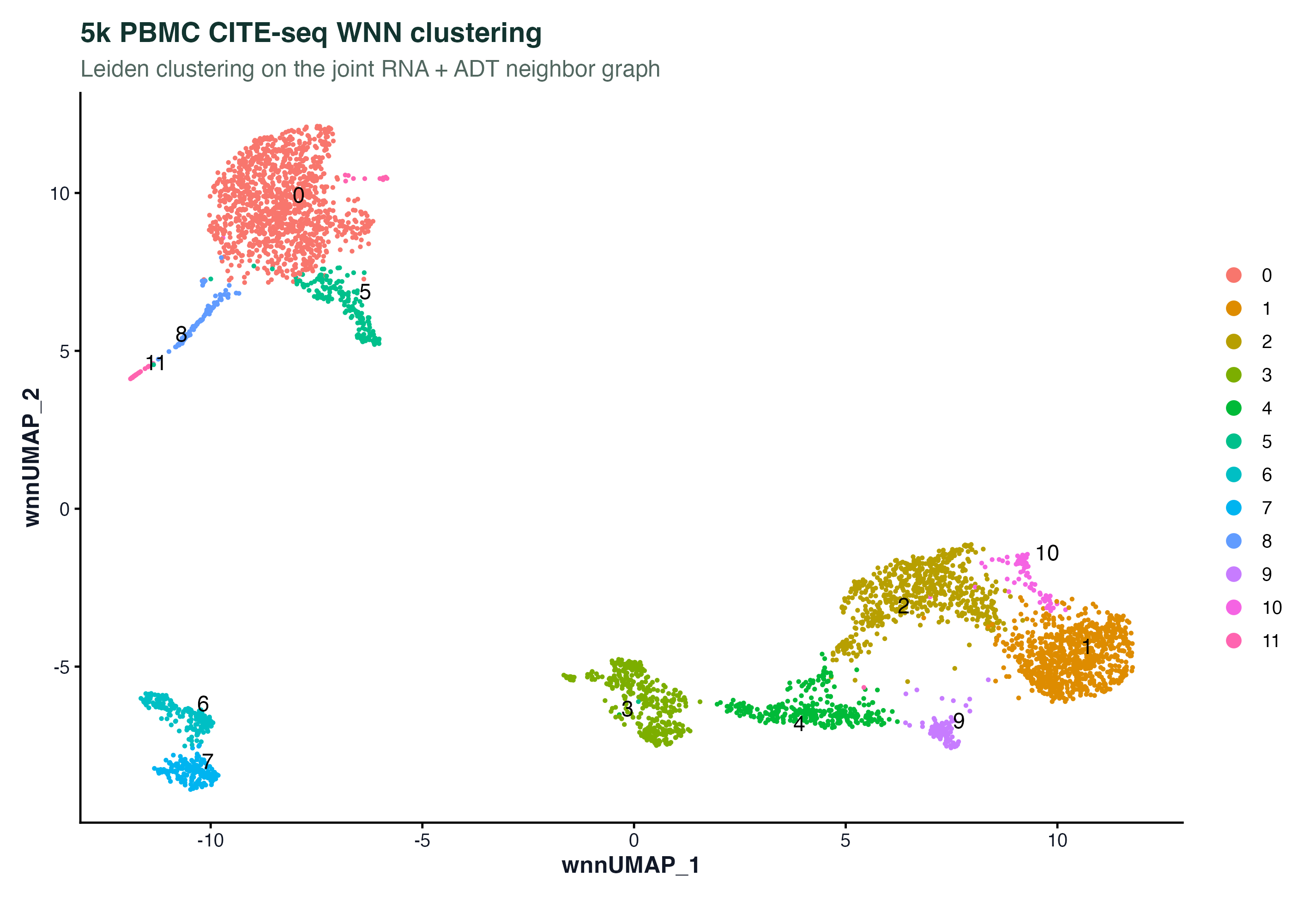
图 6:WNN UMAP 加聚类标签的完整视图。这张和单独做 RNA-only 的 UMAP 放在一起看差别最大:某些在 RNA 里贴得很近的群体(比如 CD4 memory 和 CD4 naive、CD8 effector 和 CD8 central memory)在 WNN 里通过 CD45RA/CD45RO 和 CD62L 的蛋白信号区分出来了。
套到自己数据上
脚本对 ADT 抗体名做了宽松匹配(^CD3[-_] 同时兼容 CD3_TotalSeqB 和 CD3-TotalSeqB 两种写法)。自己的 panel 只要还是 CD3/CD4/CD8/CD14/CD19/CD56 这类常规抗体名,直接跑通图 3 和图 4 的概率很高。panel 完全不同(比如肿瘤免疫的 checkpoint panel)的话,把 adt_markers 里的 CD 改成自己关心的抗体即可。nfeatures、dims.list、resolution 这三个参数按样本量调,其余不用动。
后续可做的分析
- 按蛋白 marker 重新注释聚类:PBMC 的 ADT panel 一般包含 CD3/CD4/CD8/CD19/CD14 等经典标志,比起光靠 RNA 标记,注释会更可靠。
- 找差异蛋白:
FindMarkers(cbmc, assay = "ADT", ...)可以直接在 ADT 层做差异分析。 - 与原章节对比:把这份数据的 WNN 聚类结果和 04 章里只做 RNA 的整合结果画到一起,能看到蛋白信号如何修正 RNA-only 的分群。
10x Multiome(RNA + ATAC)分析思路类似,但 ATAC 层要用 Signac,归一化方法是 TF-IDF + SVD,后面在 10 scATAC-seq 分析 里会再讲。
下载资源
参考资源
离线资料下载
手册 HTML / PDF 已在后台预生成,点击后直接下载网站静态资源。