05 多时间点与 LRT 检验
前几章�做的都是"两组比较":对照 vs 处理。真实项目里经常遇到更复杂的设计 —— 一条时间曲线,剂量梯度,多个处理条件 —— 这时候两两 Wald 检验就不够了。DESeq2 给出了两个重要工具:
- 设计公式里加交互项:
~ strain + minute + strain:minute,同时估计主效应和交互 - LRT(似然比检验):检验"完整模型相比简化模型是否显著更好拟合",一次拿到所有交互项的综合 p 值
本章用 fission 数据做演示 —— 裂殖酵母在氧化应激下的时间序列:野生型 vs atf21del 突变体,6 个时间点(0/15/30/60/120/180 min),每个组合 3 个生物学重复,共 36 个样本。
Wald 检验不够用的时候
DESeq2 的默认 results() 做的是 Wald test,回答"某一个对比(contrast)的效应是否显著"。如果问题是:
- "是否存在任何一个时间点上两个菌株有差异?" — Wald 做不了,要对每一对时间点都检验再合并 p 值,麻烦且不严格
- "药物剂量和基因表达是否有剂量-响应关系?" — Wald 只能看某两个剂量的对比
- "某条通路的变化在治疗组和对照组里是否不同?" — 这就是典型的交互项问题
LRT 的解决办法是:给一个"完整模型"和一个"简化模型",问数据在完整模型下的似然是否显著高于简化模型。如果是,说明完整模型里多出来的那些参数(通常是交互项)承载了真实信号。
具体到 fission:
# full 包含交互项、reduced 不包含
dds <- DESeqDataSet(fission, design = ~ strain + minute + strain:minute)
dds <- DESeq(dds, test = "LRT", reduced = ~ strain + minute)
res_lrt <- results(dds)
res_lrt 里每个基因的 padj 回答的是:这个基因对时间的响应,是否依赖菌株? 答案显著的基因就是"时间响应被 atf21 影响的基因"。
真实示例:fission 时间序列
配套脚本 bulk05_timecourse_sci.R 加载 fission → 建立含交互的设计 → LRT 检验 → 画 6 张图:
Rscript scripts/bulk05_timecourse_sci.R
fission 这份数据在"时间主效应"上信号非常强(细胞受到氧化应激),但 strain:minute 的交互信号比较弱(atf21 对响应的影响不那么戏剧)。实际跑下来 LRT 在 padj < 0.05 下只过了几个基因 —— 这本身就是一个重要的教学点:强交互不是所有生物学问题都存在。
图 1:PCA 看整体结构
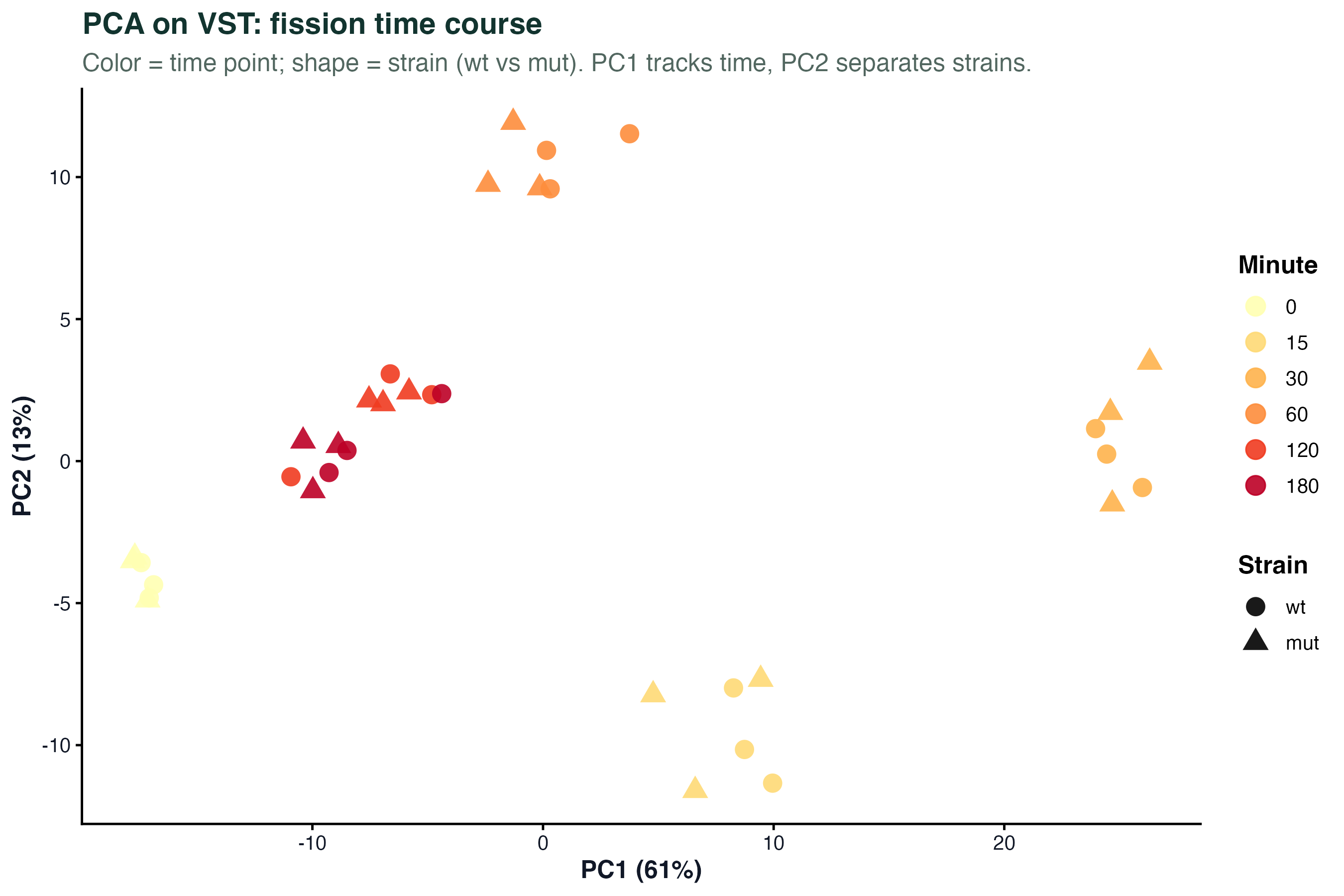
颜色表示时间,形状区分菌株。PC1 几乎就是时间轴 —— 从 0 min(浅色)到 180 min(深红),样本沿着一条轨迹排开。PC2 上两个菌株有一定分离,但比 PC1 上的时间效应弱得多。
这张图回答的第一个问题:时间是最主要的变异来源,说明设计公式里把 minute 当主效应是对的。
图 2:LRT p 值分布与统计量
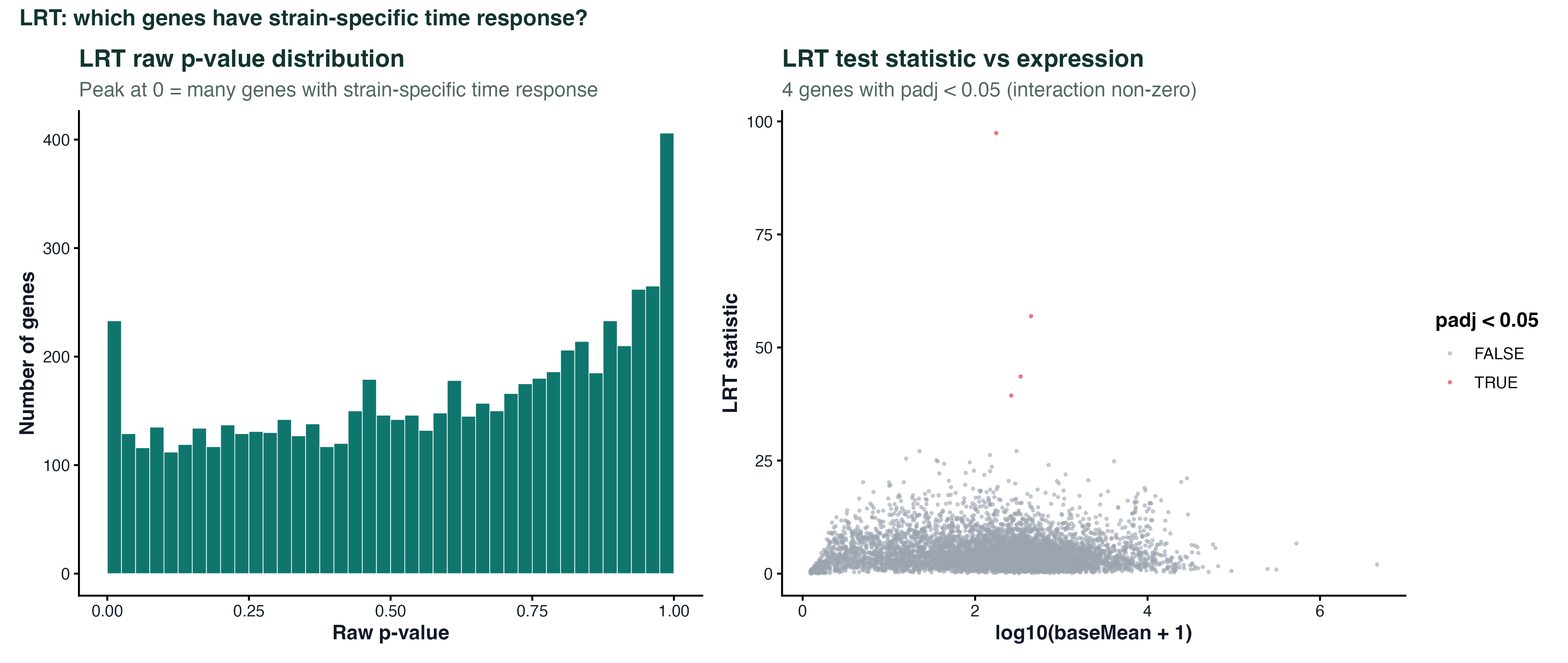
左边是 LRT 原始 p 值的直方图。和 Wald 的直方图一样:0 附近有 peak 说明有真信号,剩余部分接近均匀。 右边横轴是 log10(baseMean),纵轴是 LRT 统计量。LRT 统计量越大说明"完整模型比简化模型好"的程度越强。高表达基因(右侧)通常统计量更大 —— 这是 RNA-seq 的常见现象:高表达基因数据多、功效高。
图 3:Top LRT 基因的时间轨迹
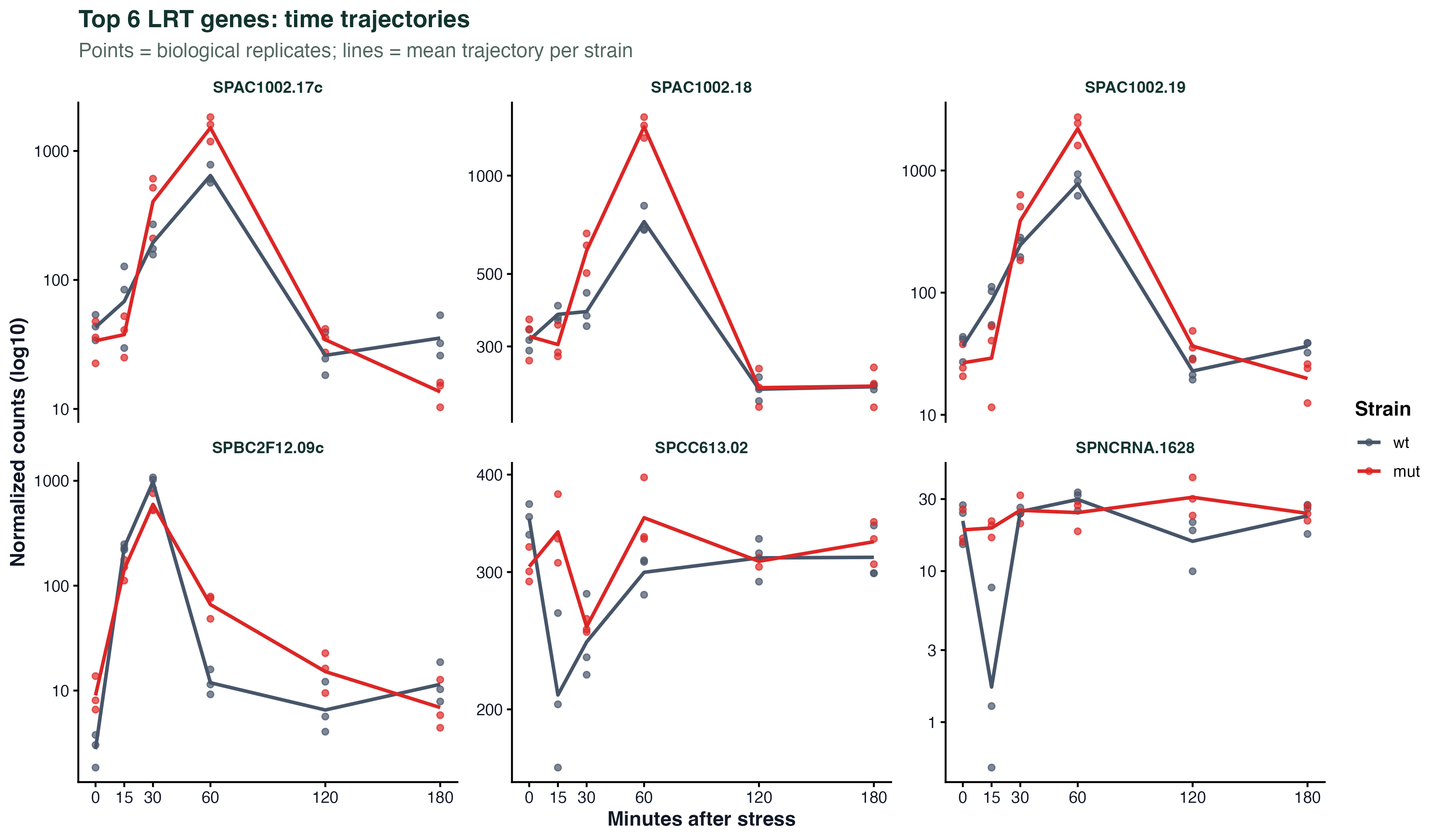
对 padj 最小的 6 个基因,把两个菌株的 normalized counts 画成时间曲线(点 = 重复,粗线 = 同时间点的均值)。可以看到 wt 和 mut 的曲线在某些时间点"分叉" —— 这就是 LRT 捕获的信号:两条曲线的形状不一样。
这种图在写论文时是"讲故事"最核心的图:把抽象的 LRT 统计量具象成"这个基因在 30 分钟的时候开始在突变体里下降"。
图 4:聚类的时间轨迹
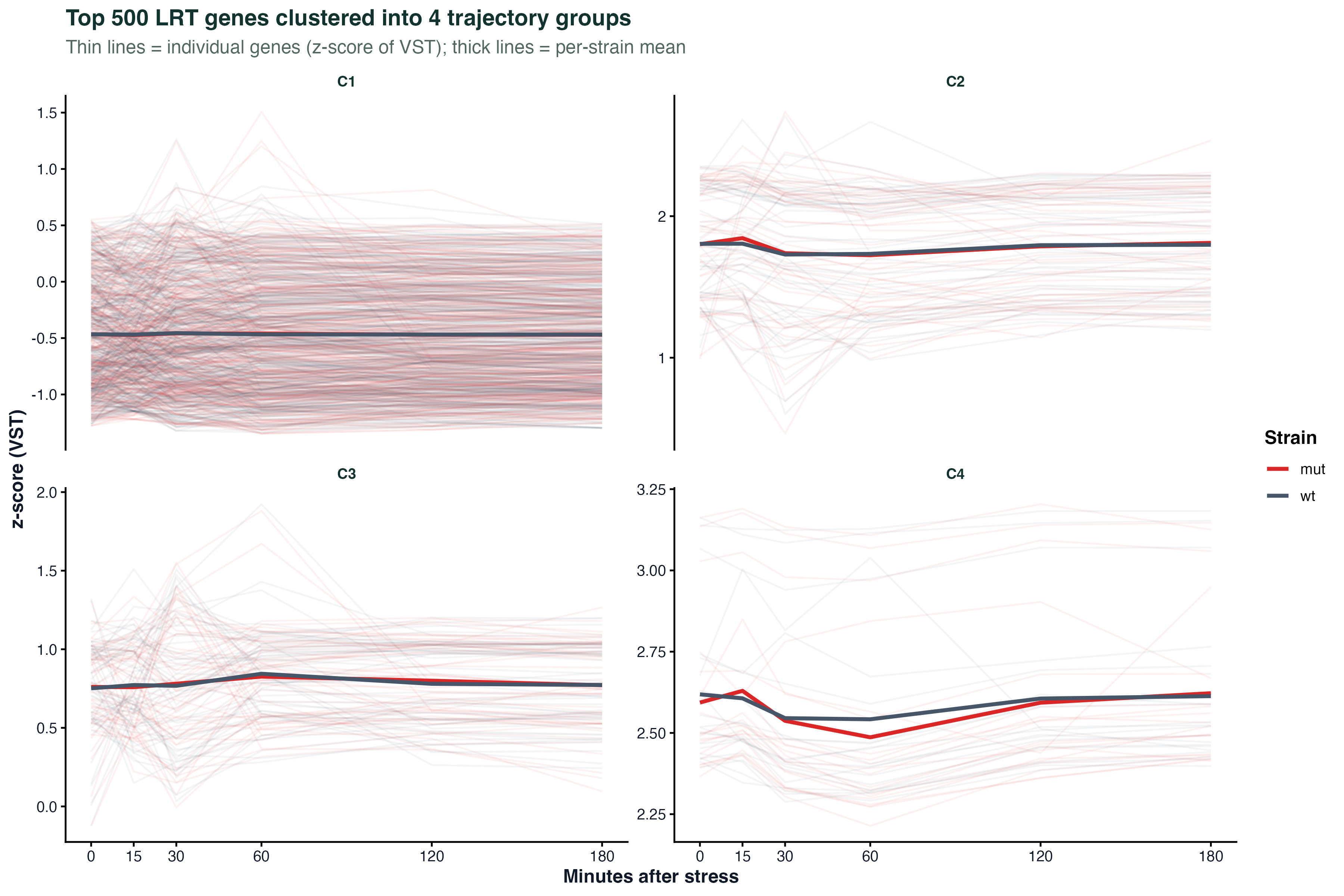
取 LRT 排名前 500 的基因,做一次层次聚类,分 4 组。每组里每个基因画一条半透明细线(z-score),最上面的粗线是两个菌株各自的均值。
这张图的信息量很大:
- 哪些基因"早响应、早下降"(C1)
- 哪些"晚响应、持续升高"(C3)
- 哪些在两个菌株间方向一致但幅度不同(C2)
- 哪些在一个菌株里响应、另一个菌株里不响应(C4)
真实项目里这张图往往比 dotplot 更能直接生成生物学假设。
图 5:特定时间点的交互 volcano
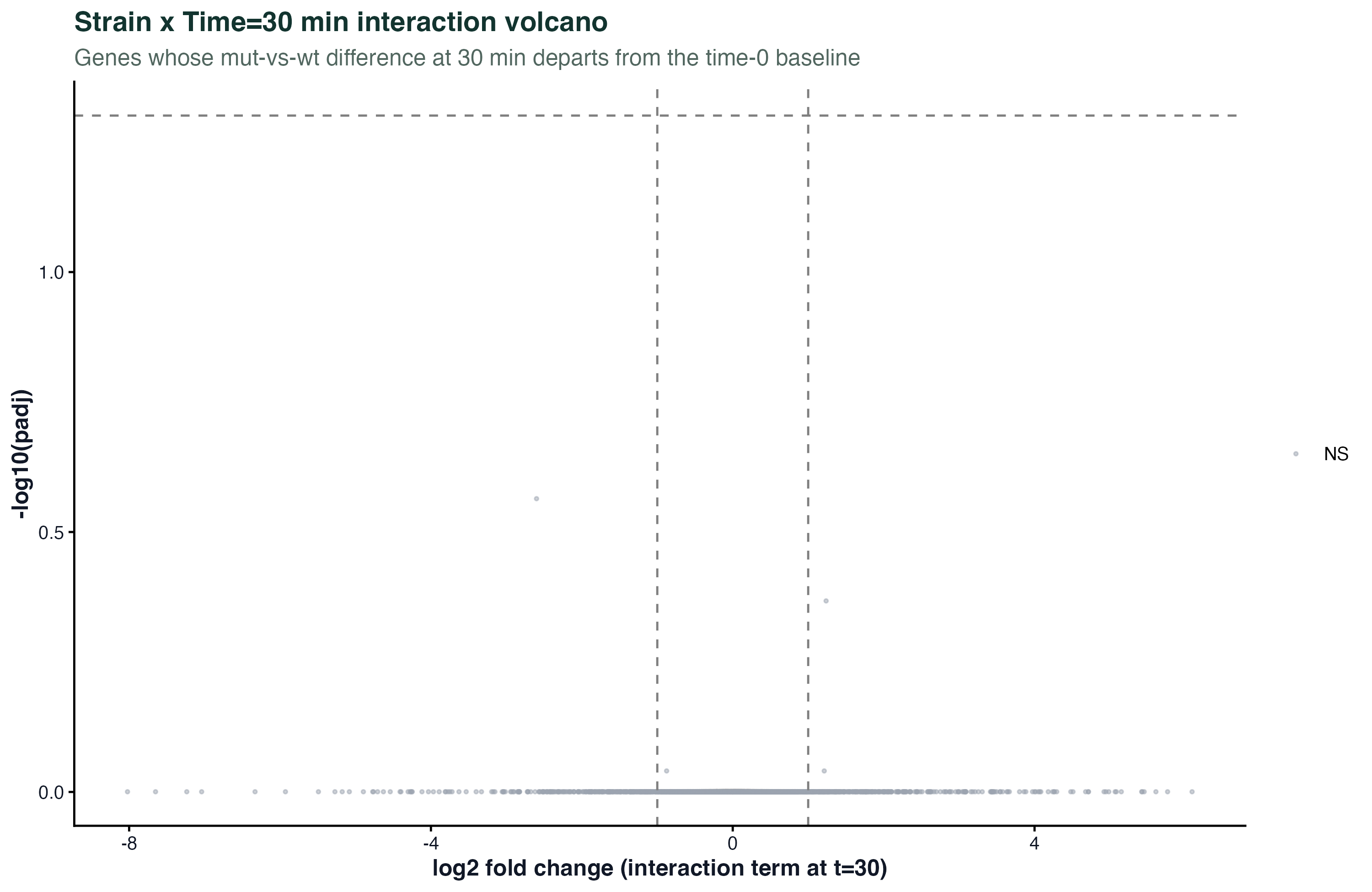
LRT 告诉你"哪些基因的响应依赖菌株",但不告诉你在哪个时间点差异最大。要定位具体时间点,改用 Wald 检验提取单独一个交互项的效应:
dds_wald <- DESeq(dds) # default test = "Wald"
# 查 resultsNames(dds_wald) 看有哪些系数
res30 <- results(dds_wald, name = "strainmut.minute30")
strainmut.minute30 这个系数回答的是:在 30 分钟时,mut 和 wt 之间的差异,相对于时间 0 的基线差异,是否显著? 正值 = mut 在 30 分钟比 wt 升得更多;负值 = mut 升得更少或反而下降。
图 6:Top LRT 基因热图(按时间排序)
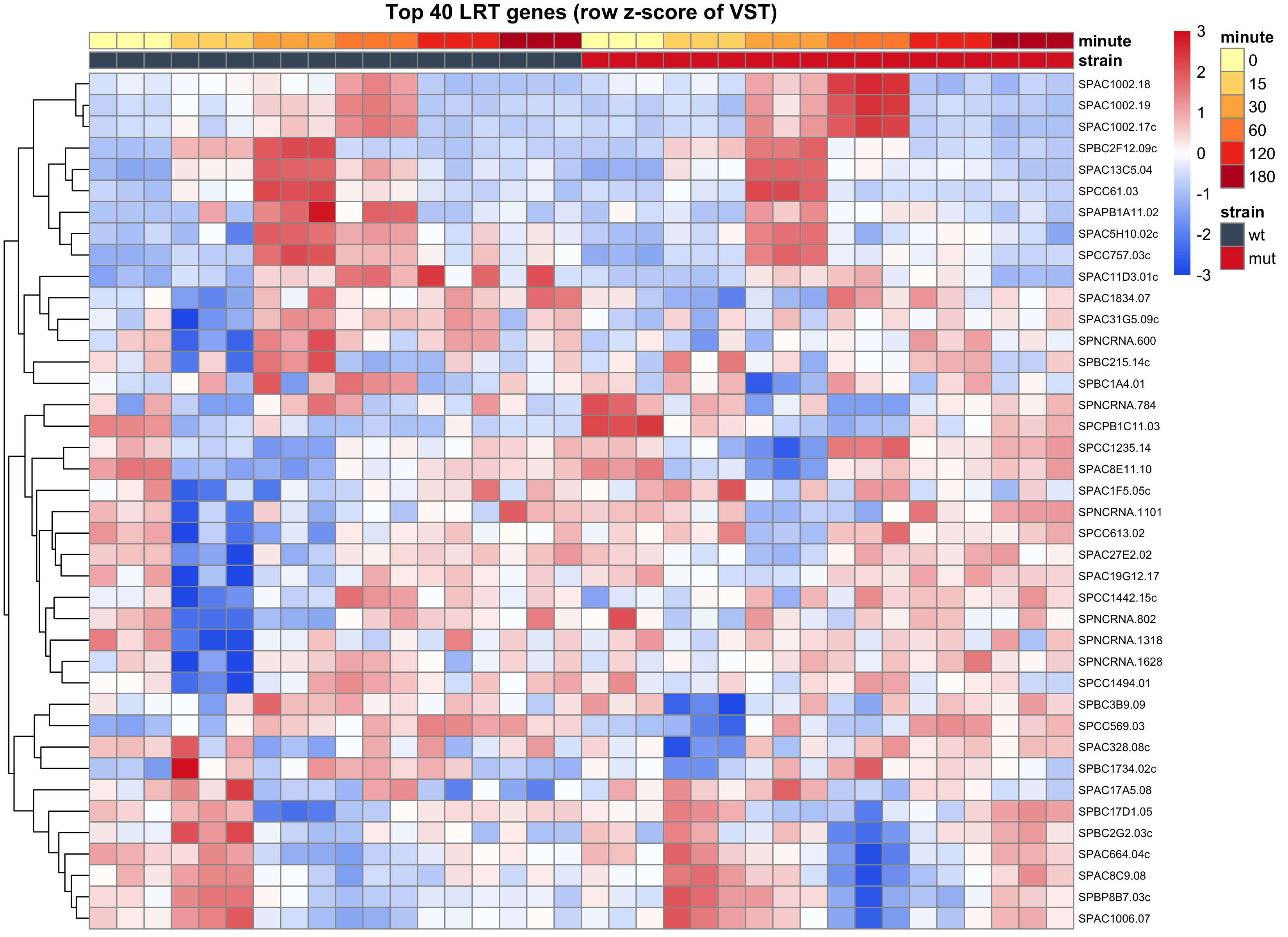
列按菌株 + 时间排序(不做列聚类),��行是 top 40 LRT 基因的 row z-score。横向左到右能看到每个基因沿时间的变化;纵向看哪些基因变化模式相似。
其他常见的复杂设计
设计公式的写法对应生物学问题。一些速查:
| 问题 | design | 检验方式 |
|---|---|---|
| 两组比较 | ~ condition | results(dds, contrast = c("condition","B","A")) |
| 控制批次 | ~ batch + condition | 同上 |
| 时间效应 | ~ minute(因子) | LRT: reduced = ~ 1 |
| 时间 × 菌株交互 | ~ strain + minute + strain:minute | LRT: reduced = ~ strain + minute |
| 连续剂量响应 | ~ dose(数值变量) | Wald on dose coefficient |
| 多条件 + 批次 | ~ batch + tissue + condition | results(..., contrast = ...) |
两个关键原则:
- 要检验的变量一般放 design 最后,results() 默认取它
- LRT 时
reduced要和full只差你关心的那些项 —— 差得越多,LRT 就是在同时检验那些项的组合,解读会变乱
和 single-cell 的对比
单细胞里做"轨迹推断 + 沿拟�时序的差异"(比如 Slingshot + tradeSeq),思路和 bulk 里 LRT 很像:都在问"基因表达是否沿着某个连续变量系统性变化"。主要差别:
- bulk 的 minute 是实验里设好的时间点,维度离散、样本多;单细胞的 pseudotime 是推断出的连续变量,每个细胞一个值
- bulk 的 LRT 基于 counts 的负二项分布;
tradeSeq用 GAM 拟合连续轨迹
下载资源
下一步
参考资源
离线资料下载
手册 HTML / PDF 已在后台预生成,点击后直接下载网站静态资源。